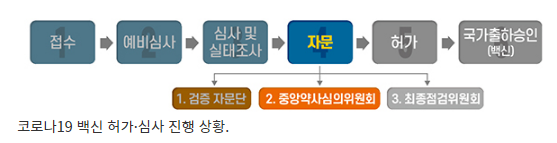
국내개발 1호’ 코로나19 백신 중앙약심 통과…“품목허가 가능” SK바이오사이언스사 개발·제조…최종점검위원회 허가 여부 최종결정 2022.06.27 식품의약품안전처 ‘국내개발 1호’ 코로나19 백신이 중앙약사심의위원회를 거쳐 ‘최종점검위원회’의 허가 여부만 남겨놓게 됐다. 오일환 중앙약사심의위원회 위원장은 27일 “SK바이오사이언스사의 ‘스카이코비원멀티주’(개발명, GBP510)를 품목허가할 수 있다고 의견을 모았다”고 밝혔다.
이날 코로나19 백신 중앙약사심의위원회 자문 결과 브리핑에 나선 오 위원장은 “스카이코비원멀티주의 안전성과 효과성에 대해 자문하기 위해서 중앙약사심의위원회를 지난 26일 개최했다”면서 이같이 말했다. 이어 “현재까지 임상시험에서 발생한 이상사례 등의 안전성은 허용할 수 있는 수준으로 판단했다”면서 “효과성 면에서도 품목허가가 가능하다고 판단했다”고 덧붙였다.
이에 따라 식품의약품안전처는 향후 전문가 의견과 효능·효과(안), 용법·용량(안), 권고사항 등을 종...
#GBP510
#코로나19백신중앙약심통과
#코로나19백신
#최종점검위원회
#중앙약사심의위원회
#중앙약사심의위원
#중대한이상사례
#식품의약품안전처
#스카이코비원멀티주
#스카이코비원멀티
#백신투여
#백스제브리아주
#글로벌공급
#국내개발1호
#SK바이오사이언스
#확보방안
원문링크 : 국내개발 1호’ 코로나19 백신 중앙약심 통과…품목허가 가능(SK바이오사이언스사 개발·제조…최종점검위원회 허가 여부 최종결정)


![[과학기술정보통신부 ] 공공 상용 소프트웨어 구매비율 2025년 20%로 높인다(과기부 ‘소프트웨어 경쟁력 강화 추진전략’ 마련)](https://mblogthumb-phinf.pstatic.net/MjAyMTA2MThfMTcw/MDAxNjIzOTc1MjcwMDI0.B8ZB-Dm83yDQwmaPOQoslpDN8W5GxzXnuN25ibHTY50g.MSJA4TZv6xWJzDse73pZgww4nPkKiwYeBE8mKAgzpWsg.PNG.ash1106/image.png?type=w2)

![[뉴스] 이별통보 여친 흉기로 살해 26세 김레아…검찰, 머그샷 첫 공개](https://mblogthumb-phinf.pstatic.net/MjAyNDA0MjJfNzkg/MDAxNzEzNzkwMjUyNTE4.5UblD6z3F-k1P8TCYfkEyTJ4-qVTxevq2YWWVessKBcg.mjHjQ_YImxxWwFOh-fvWzT7hLsVsnafahDYjb6NFvlcg.PNG/image.png?type=w2)

![[세종] 2021년 지역기업 혁신성장 바우처지원사업 참여기업 모집 공고](https://mblogthumb-phinf.pstatic.net/MjAyMTA4MTdfMjkg/MDAxNjI5MTg5MDAyOTE4.7NwFZfH4yBJmFFvRvm4hNEURN2WToj60ZM2pIXjco_Eg.__5G9f_WBM7R2bChEB_V1vcCr8wNnYzJjg8lMYI1nwEg.PNG.ash1106/image.png?type=w2)

 네이버 블로그
네이버 블로그 티스토리
티스토리 커뮤니티
커뮤니티