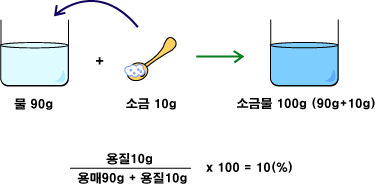
# 화학I # 1. 화학의 첫걸음, # 5. 퍼센트농도와 몰 농도 퍼센트농도는 용질(녹아있는 물질)과 용액의 질량의 비율입니다. 하지만, 이런 단점이 있습니다. 화학식을 만드는데 가장 중요한 것은 '몰 수' 인데요. 그러나, 퍼센트농도로는 몰 수를 계산하기 복잡하고 같은 퍼센트농도여도 물질의 '양'이 달라요. 매번 계산해서 분수를 어쩌고 저쩌고... 하기 너무 힘들잖아요? 그래서 화학식을 편하게 쓰기 위해 '몰 농도'라는 개념을 만들었어요. 몰 농도는 용액 1L에 녹아 있는 물질의 몰 수 입니다. 이 때의 단위는 mol/L 또는 M을 씁니다. 1mol/L = 1M = 1L에 1몰의 입자가 있는 경우. 말로 백날 설명해봤자 글로는 100% 전달이 불가능하죠. 문제를 만나보시면 이해가 훨씬 쉬우실 겁니다. + 아보가드로 법칙에서 22.4L에 1mol의 입자가 있었죠? 그러니까 1L에 들어 있는 입자 수는 0.0몇 정도로 작은 값인 경우가 많답니다. 계산이 무슨 0.0025M 이따구여도 ...
원문링크 : 1-5. 퍼센트농도와 몰농도

 네이버 블로그
네이버 블로그 티스토리
티스토리 커뮤니티
커뮤니티