
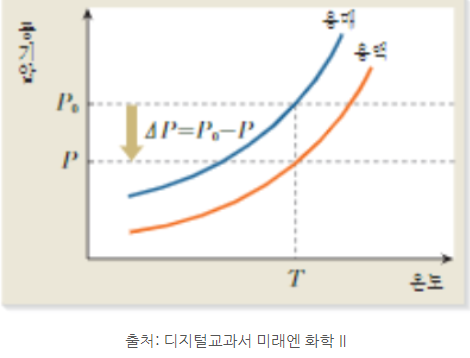
돌턴의 부분 압력 법칙 공식입니다. 사실 매우 간단한 내용이지만, 뭔가 있어보이는 문자로 써놓으니까 어렵게 느껴져요. 간단하게 예시를 들어서 살펴볼게요. 1기압의 산소 1L 와 2기압의 질소 1L 를 섞었어요. 이 때, 전체 기체의 압력은 어떻게 계산할까요? 여기서 우리가 고려해야 하는 것은 부분 압력이라는 개념입니다. 부분 압력은 어떤 기체가 전체에서 나타내는 압력을 의미합니다. 예를 들어, 위의 문제에서 1기압 산소는 혼합 기체에서 0.5기압으로 옅어졌고 2기압 질소는 혼합 기체에서 1.0기압으로 옅어졌어요. 두 기체를 합치면서 부피가 2배로 늘었으니 압력은 절반으로 줄어든거죠. 보일 법칙이고요. 보일 법칙 # 화학 II # 1. 물질의 세 가지 상태와 용액 # 1. 기체의 성질 보일 법칙은 중1 과학에서 배웠던 내용인... blog.naver.com 여기서, 혼합 기체에서 산소의 압력 0.5기압을 산소의 부분 압력. 혼합 기체에서 질소의 압력 1.0기압을 질소의 부분 압력이라고...
원문링크 : 돌턴의 부분 압력 법칙


 네이버 블로그
네이버 블로그 티스토리
티스토리 커뮤니티
커뮤니티