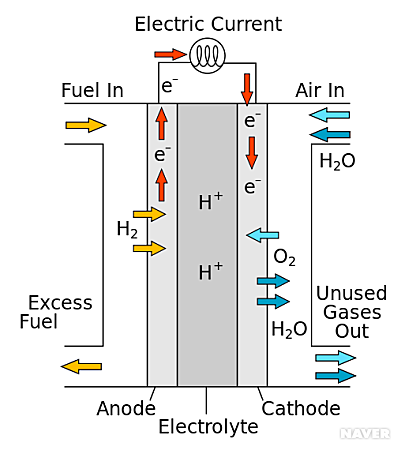
연료 전지의 가장 기본적인 형태로 수소를 산화 전극의 연료로 사용한다. 작동 원리 수소와 산소가 반응하여 물이 되는 전체 반응 (2H2 + O2 → 2H2O)을 통해 전자는 산화전극(anode)에서 외부 도선을 통해 환원전극(cathode)으로 이동하면서 전기 에너지를 발생시킨다. 산성 또는 염기성 전해질 조건에서 산화 및 환원전극의 반응은 아래와 같다. 산화전극에서 연료인 수소의 산화 반응이 일어난다. 2H2 → 4H+ + 4e- (산성 조건) 2H2 + 4OH- → 4H2O+ 4e- (염기성 조건) 환원전극에서는 산소의 환원 반응이 일어난다. O2 + 4H+ + 4e- → 2H2O (산성 조건) O2 + 2H2O + 4e- → 4OH- (염기성 조건) 산성 조건에서 수소 이온이 이동할 수 있는 고분자 막을 전해질로 사용하는 경우를 고분자 전해질 연료 전지라고 하며, 30-40% 농도의 수산화 포타슘(KOH) 용액을 전해질로 사용하는 경우를 알칼리 연료 전지라고 부른다 실제 전기 ...
원문링크 : 수소연료전지 (Hydrogen fuel cell)




 네이버 블로그
네이버 블로그 티스토리
티스토리 커뮤니티
커뮤니티