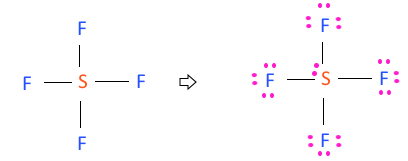
【 목 차 】 1. 분자의 루이스 구조 2. 전자쌍 반발 이론 3. 결합각과 분자의 구조 4. 극성분자와 무극성 분자 5. 분자간 힘 1. 분자의 루이스 구조 단계 1. 분자에 있는 전체 원자가 전자의 수를 구한다. 단계 2. 원자 사이를 단일 결합으로 연결한다. (중심원자는 수소를 제외하고 전기음성도가 제일 낮은 원자로 정하고 2주기 원소들을 팔전자 규칙을 만족하도록 결합수를 정한다. 붕소(B)는 예외적으로 전자 결핍이 되고, 3주기 이상의 원소들은 d오비탈의 영향으로 확장된 팔전자 규칙을 따르기도 한다) 단계 3. 단계1 에서 구한 전체 원자가 전자 수로 부터 결합에 이용한 원자가 전자수를 뺀 나머지 전자들을 전기 음성도가 큰 말단 원자에 할당하여 팔전자 규칙을 정한다. 단계 4. 단계 3 이후에도 할당되지 않고 남은 전자가 있다면 중심 원자에 배치한다. (중심 원자가 3주기 이상이면 전자를 8개 보다 많이 가질 수 있다!!!) 단계 5. 만약 중심원자가 팔전자 규칙을 만족하지 ...
#결합각
#극성분자
#루이스구조
#무극성분자
#분자
#분자간힘
#전자쌍
#평면삼각형
원문링크 : 분자의 구조와 성질 - 기초 화학


 네이버 블로그
네이버 블로그 티스토리
티스토리 커뮤니티
커뮤니티